Oxit cao nhất của ngtố Y là YO3. Trong hợp chất hiđro của Y , hiđro chiếm 5,88% về khối lượng. Y là nguyên tố?
Giải chi tiết giúp em ạ , nếu đc thì có thể giải thích dùm em lun ạ! Em cảm ơn..
Oxit cao nhất của một nguyên tố là YO3, trong hợp chất của nó với hiđro có 5,88% H về khối lượng. Vị trí của Y trong bảng tuần hoàn:
A. Chu kì 3, nhóm VIA.
B. Chu kì 3, nhóm IVA
C. Chu kì 2, nhóm VIA
D. Chu kì 4, nhóm IIA
Đáp án A
Vì công thức oxit cao nhất của Y là YO3
Nên công thức hợp chất khí của Y với hidro là YH2.
Khi đó phần trăm khối lượng của H trong YH2 là:
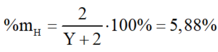 Y = 32 là S
Y = 32 là S
Do đó vị trí của Y trong bảng tuần hoàn là chu kì 3, nhóm VIA
Cho hợp chất Z của nguyên tố A có hóa trị là II, với nguyên tố Oxi, biết nguyên tố oxi chiếm 20 phần trăm về khối lượng, tên của nguyên tố A ( mn giải chi tiết ra giúp em vs ạ, em cảm ơn nhiều )
CTHH của Z là : \(AO\)
\(\%O=\dfrac{16}{A+16}\cdot100\%=20\%\)
\(\Rightarrow A=64\)
\(A:Cu\) ( Đồng )
Oxit cao nhất của một nguyên tố R là RO3, trong hợp chất của nó với hiđro có 5,88% hiđro về khối lượng. Xác định nguyên tố R
Nguyên tố 'R' có oxit cao nhất là R2O3, => Hóa trị cao nhất của 'R' là 6
Hóa trị thấp nhất của R trong hợp chất với oxygen + Hóa trị của R trong hợp chất
thi với hydrogen = 8
=> Hóa trị của R trong hợp chất thi với hydrogen = 8 - 6 = 2
=> Công thức hợp chất thi với hydrogen là RH2
Ta có: %MH(R+H2) = (2/(R+2)) * 100
=> 5,88 = (2/(R+2)) * 100
=> R = 32
=> R là Sulfur (S)
Oxit cao nhất của nguyên tố Y là YO3. Trong hợp chất với hiđro của Y, hiđro chiếm 5,88% về khối lượng. Y là nguyên tố
A.O
B.P
C.S
D.Se
Y có hóa trị II hoặc VI, nếu hóa trị II → H2Y → 2/(2 + Y) = 0,0588 → Y = 32 (S).
Oxit cao nhất của một nguyên tố là RO3, trong hợp chất của nó với hiđro có 5,88% H về khối lượng. Xác định nguyên tử khối của nguyên tố đó.
Oxit cao nhất của một nguyên tố là RO3, theo bảng tuần hoàn suy ra công thức hợp chất khí với hiđro của nó là RH2, trong phân tử RH2, có 5,88% H về khối lượng
nên R có 100 - 5,88 = 94,12% về khối lượng
Trong phân tử RH2, có: 5,88% H là 2u
94,12% R là x u
Giải ra ta có x ≈ 32. Nguyên tử khối của R = 32. R là S. Công thức phân tử là SO3 và H2S.
Hợp chất khí với hiđro của nguyên tố R la RH3. Trong oxit cao nhất của nó chứa 74.08% oxi về khối lượng . R là gì
R là nguyên tố có hợp chất khí với hiđro là RH và R chiếm 38,79% về khối lượng trong oxit cao nhất Xác định R. Nguyên tố R có 2 đồng vị là X và Y tổng số khối của 2 đồng vị này là 72 va ti le so nguyen tu cua chung la 3:1 Xac dinh so khoi X va Y
Oxit cao nhất của R có công thức R2OX. Phân tử khối của R2OX là 183 phần trăm khối lượng oxi trong R2OX LÀ 61,2% Xác định R
RH3 => a=3 => b=8-3=5
R2O5
%R2O5 = 80*100=(2R+80)*74,08 => R=14 =>R=Si
Hợp chất khí với hiđro của nguyên tố R la RH2. Trong oxit cao nhất của nó chứa 74.08% oxi về khối lượng . R là gì
R là nguyên tố có hợp chất khí với hiđro là RH và R chiếm 38,79% về khối lượng trong oxit cao nhất Xác định R. Nguyên tố R có 2 đồng vị là X và Y tổng số khối của 2 đồng vị này là 72 va ti le so nguyen tu cua chung la 3:1 Xac dinh so khoi X va Y
Oxit cao nhất của R có công thức R2OX. Phân tử khối của R2OX là 183 phần trăm khối lượng oxi trong R2OX LÀ 61,2% Xác định R
Giúp mình giải thích chi tiết bài này dễ hiểu với !
Công thức oxit cao nhất của nguyên tố R là R2O5 trong hợp chất khí với hidro, R chiếm 82,35% về khối lượng . Xác định nguyên tử khối cua nguyên tố đó ?
Help me
Công thức oxit cao nhất là R2O5
\(\Rightarrow\) Hợp chất với hidro là RH3
\(\Rightarrow\dfrac{M_R}{M_R+3}\cdot100=82,35\) \(\Rightarrow M_R\approx14\) (đvC)
Oxit cao nhất của một đơn chất R có dạng RO3. Trong hợp chất khí với hiđro thì R chiếm 97,531% về khối lượng. Nguyên tố R là
A. S
B. Se
C. P
D. Te
Đáp án B
Oxit cao nhất của một đơn chất X có dạng RO3.
⇒ Hợp chất khí với Hidro là H2R.
Ta có: 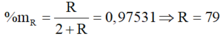
Vậy R là Se
Oxit cao nhất của một đơn chất R có dạng RO3. Trong hợp chất khí với hiđro thì R chiếm 97,531% về khối lượng. Nguyên tố R là
A. S.
B. Se.
C. P.
D. Te.
Đáp án B
Oxit cao nhất của một đơn chất X có dạng RO3.
=> Hợp chất khí với Hidro là H2R.
Ta có:
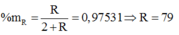
Vậy R là Se